CrossBridge Bio 由 Michael Torres 博士、Kyoji Tsuchikama 博士和 Zhiqiang An 博士于 2023 年创立,致力于推进由 UTHealth Houston 的 Kyoji Tsuchikama 博士所开发的新型双载荷 ADC 技术。
CrossBridge 的 ADC 技术平台主要包括三个创新点:EGCit(GluGlyCit)酶促可裂解linker、支链linker的酶促偶联和Antibody-Payload协同配对。
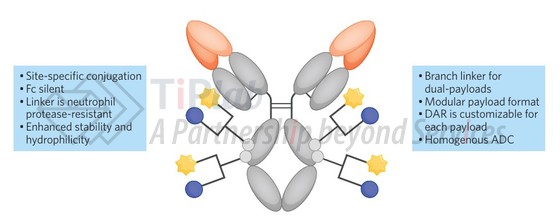
EGCit酶促可裂解linker:与传统 ValCit 连接子相比,抗蛋白酶稳定性增强且亲水性提高。
支链linker的酶促偶联:利用微生物转谷氨酰胺酶(mTG),利用点击化学将支链linker偶联至单个 hIgG1 位点,并能实现针对不同作用机制有效载荷的理性设计。
EGCit(GluGlyCit)linker
根据Kyoji Tsuchikama 2022年发表的文章,EGCit 连接子在小鼠和灵长类动物血浆中均具有长期稳定性,能抵抗人中性粒细胞蛋白酶介导的裂解,不会损伤分化的人类中性粒细胞,同时在细胞内裂解后仍能以无痕方式释放有效载荷。
- VCit 接头因其易受细胞外羧酸酯酶 Ces1c 的作用而在小鼠循环系统中不稳定,VCit 接头也易受人中性粒细胞弹性蛋白酶介导的降解。
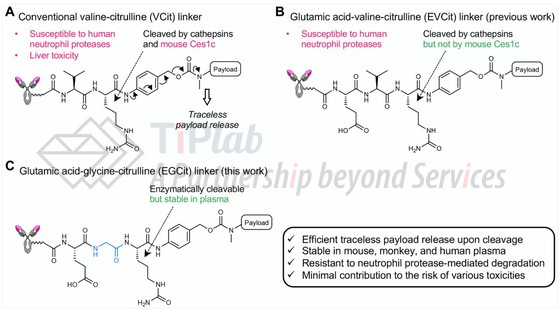
相关专利家族 PCT/US2022/082020 涉及一种三肽接头及其使用方法,权利要求限定结构通式。
支链linker
2017年,Kyoji Tsuchikama团队开发了一类支链 ADC 连接子,可通过微生物转谷氨酰胺酶(MTGase)介导的偶联反应和正交应变促进的叠氮-二苯并环辛炔(DBCO)环加成反应,将两个相同的有效载荷分子定点定量地连接到单个抗体上。
2021年,Kyoji Tsuchikama团队设计并合成了新的支链连接子(diazido-methyltetrazine tri-arm linker)以构建双载荷 ADC,其上分别带有叠氮基和甲基四嗪基作为正交点击反应手柄。另外设计了有效载荷模块作为点击反应的对应模块,包括:DBCO 或 TCO 作为点击反应对、PEG间隔臂、GluValCit可切割连接子、PABC基团,以及有效载荷本身(MMAE 或 MMAF)。
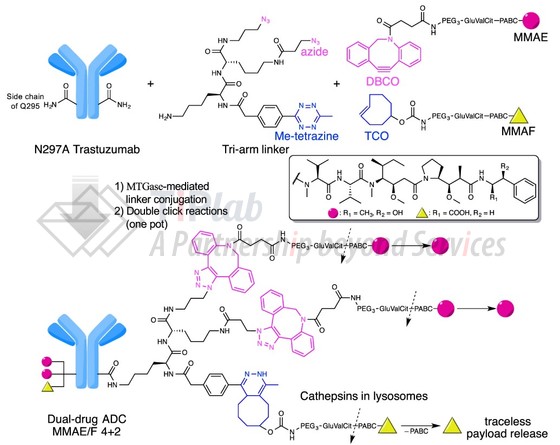
相关专利家族 PCT/US2018/034363 涉及连接子、包含其的linker-payload或ADC的结构通式。
CBB-120
基于其 ADC 平台设计的主导项目 CBB-120 是一种靶向 TROP2 的 ADC,结合了拓扑异构酶 I 抑制剂(TOP1i)和 ATR 抑制剂(ATRi)两种有效载荷,与目前 TROP2 靶向 ADC 相比(吉利德的 Trodelvy 以及阿斯利康/第一三共的 Datroway 均已获批上市),CBB-120 旨在提高治疗指数并产生更持久的疗效,同时还能解决关键的耐药机制。计划于 2026 年向FDA 递交 IND。
以Kyoji Tsuchikama为发明人的一个专利家族PCT/US2025/014102涉及TROP2靶向的抗体或包含其的ADC。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
