Tubulis 致力于开发下一代 ADC,总部位于德国,此次协议是在吉利德与 Tubulis 开展两年合作的基础上达成的。
Tubulis的技术平台主要包括三种技术:P5 缀合技术(乙炔基膦酰胺接头偶联)、Tubutecan(基于exatecan的linker-payload)和Alco5(基于磷酰胺的自裂解连接子单元)。
2026年1月,Tubulis 在 Nature Communications 上发表了关于 Alco5 偶联平台扩展 ADC payload空间的研究成果,文中提出了一种基于磷酰胺的自裂解连接子单元,其能够在血清中保持稳定,并在靶细胞内实现脂肪醇和芳香醇类药物的“无痕释放”(traceless release)。这类连接子能够实现抗体与一类此前难以连接的含羟基payload(包括具有蛋白降解等新型作用机制的载荷)的连接(相关专利家族:PCT/EP2023/087529)。Alco5 通过引入全新的payload类型与 Tubulis 的 P5 平台形成互补,从而帮助解决耐药性问题。
作者借鉴了临床已验证的 ProTide 技术并重新设计了磷酰胺基团的中心磷原子,在其三个取代基之一上引入共轭基团,该基团可以与抗体等靶向基团形成共价键。
- ProTide 技术是一种前药系统,旨在掩盖核苷类药物分子的亲水性,从而增强其细胞渗透性,基于该技术已成功开发出包括sofosbuvir在内的三种抗病毒药物。
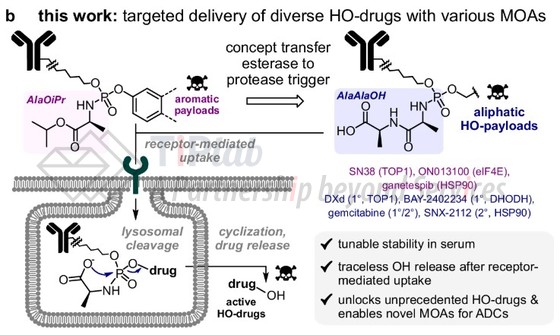
这种基于磷酰胺的自裂解连接子可用于递送多种脂肪醇和芳香醇类payload,并通过多种细胞内和内体触发因素(包括酯酶、蛋白酶、葡萄糖醛酸酶和还原条件)启动释放,图中展示了酯酶触发连接子AlaOiPr-(粉色背景)和蛋白酶触发连接子AlaAlaOH-(紫色背景)。
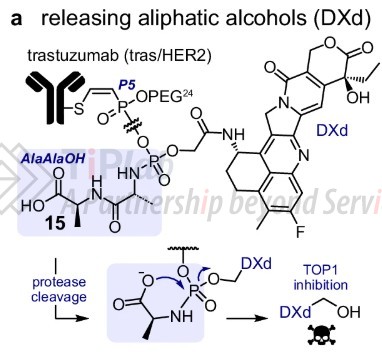
其中,作者以 DXd 作为模型有效载荷构建了ADC:曲妥珠单抗(tras/抗 HER2)衍生的 DAR8 ADC,采用 DXd 和蛋白酶可切割释放接头(紫色背景,通过五元环化启动释放)。
Tubulis 的主要资产 TUB-040 是一种靶向 NaPi2b 的拓扑异构酶 I 抑制剂(TOPO1i)ADC,目前正处于铂耐药卵巢癌和非小细胞肺癌(NSCLC)的 Ib/II 期临床开发阶段。另一款候选产品 TUB-030 是一种靶向 5T4 的 ADC,已在多种实体瘤类型中展现出令人鼓舞的初步临床数据。
关于Tubulis技术和产品的更多介绍和相关专利情况可参见往期文章《Tubulis的下一代 ADC 技术》,此处不再赘述。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
