Foundayo(orforglipron)是在 FDA 的专员国家优先审评券(CNPV)试点项目下的第五个获批项目。该批准在申报后仅 50 天即作出,较FDA的法定审评截至时间(2027 年 1 月 20 日)提前了 294 天,是该项目下首个新分子实体(NME)的获批,具有里程碑意义。这也是自 2002 年以来,新分子实体获批速度最快的一次。
在 ATTAIN 临床试验项目的支持下,Foundayo 已被证实能够帮助人们减轻体重并保持体重。在 ATTAIN-1 试验中,服用最高剂量 Foundayo 并坚持治疗的受试者平均减重 27.3 磅(12.4%),而安慰剂组仅减重 2.2 磅(0.9%)。据 Cortellis 数据库显示,分析师预测该药物到 2030 年的销售额将超过 150 亿美元。
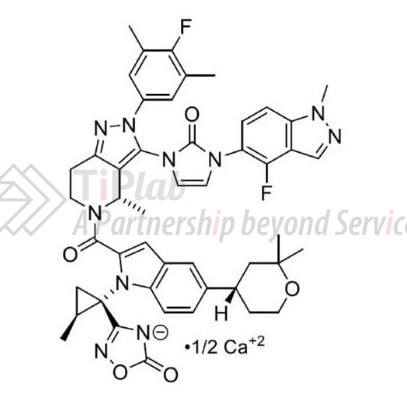
除用于慢性体重管理外,orforglipron 目前还在研究其作为 2 型糖尿病、阻塞性睡眠呼吸暂停、骨关节炎膝关节疼痛、高血压、外周动脉疾病和压力性尿失禁的潜在治疗药物。更多orforglipron的介绍请参见往期文章《礼来的口服 GLP-1 受体激动剂 orforglipron》。
礼来将与诺和诺德在口服减肥药市场展开正面竞争。这两款口服药物虽然疗效不如注射剂,但在使用便利性方面更具优势。诺和诺德已获批每日一次的司美格鲁肽口服制剂需在早晨空腹服用,且服药后 30 分钟内不得进食或饮水。Orforglipron 也是每日一次,但服药时间不受进食或饮水限制。
小分子 GLP-1 受体激动剂领域持续受到关注,比如,2026 年 3 月中旬,Structure Therapeutics 公布了其每日一次口服小分子 aleniglipron 的疗效(180 mg组44周平均减重16.3%)与注射用 GLP-1 受体激动剂疗效相当(参见往期文章《Structure 的口服小分子 GLP-1 受体激动剂 aleniglipron》)。2026年3月底,Ambrosia 获得 1 亿美元 B 轮融资,将把下一代口服 GLP-1 推进至临床试验,根据官网披露,其重点在于降低人体有效给药剂量、实现 24 小时靶点覆盖,并提升联合用药的兼容性。
在专利视角,该领域也十分拥挤,比如,2025年12月,罗氏通过 1 亿美元专利许可提前解决GLP-1在研药物的潜在专利障碍(参见往期文章《罗氏通过 1 亿美元专利许可提前解决GLP-1在研药物的潜在专利障碍》)。在国内,2025年6月,石药对歌礼的美国授权专利US12234236B1发起PGR挑战(PGR2025-00057),US12234236B1保护7个具体的结构式,与orforglipron的结构类似。歌礼表示,石药尚在专利申请中的化合物10(PCT/CN2024/140920)与US12234236B1所涵盖的化合物1的分子结构完全一致,但歌礼向USPTO提交专利申请的日期领先石药申请的日期3个多月。

* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
